생체 시뮬레이터에서 선택적 누출 폐쇄에 대한
생체재료의 부착강도 실험 평가
Evaluating the in vitro Adhesive Strength of Biomaterials.
Biosimulator for Selective Leak Closure
Carbon RT, Baar S, Kriegelstein S, Huemmer HP, Baar K, Simon S-I
Biomaterials. 2003;24:1469-75
ABSTRACT
목적: 수술은 지혈과 조직관리 면에서 항상 문제를 야기할 수 있다. 훌륭한 임상적 타당성(relevance)을 나타낸 액상 밀폐제와 플리스(fleece-bound) 밀폐제의 부착강도에 대한 지식으로 조직 밀폐를 하고자 한다. 압력챔버(생체 시뮬레이터) 안의 생체막(biomembrane)에 대해 표준화된 방법으로 기술적이고 생체역학적으로 실험해 온 것과 같이 누출 폐쇄 모델을 적용하였다.
발견: 액상 밀폐제(피브린 접착제[fibrin gluing]: 4.1 hPa, 광중합성[photopolymerisate]: 82.9 hPa)는 최저와 최고의 부착강도를 나타내었다. 플리스 밀폐제(fleece-bound sealing)는 순수 액상 밀폐제에 비해 운반체와 상관 없이 안정적이었다. 피브리노겐 코팅이 돼있어 ‘ready-to-use’가 가능한 생분해성 콜라겐 시스템인 TachoCombⓇH에 비해 사용 시점에서(on the spot) 코팅을 해야 하는 액상 밀폐제(prepare-to-use: 22.3-25.3 hPa)의 부착강도는 유의하게 낮았다(p‹0.0001). 실용성과 유효성 및 효율성 면에서 ‘ready-to-use’ 시스템의 장점이 크다.
결론: 이 연구에서 사용한 생체 시뮬레이터는 조직 관리(tissue management)에 적용이 가능하고 재현이 가능하며 조직 밀폐와 같은 복구체계에 대해 경제학적이고 생태학적인 평가를 가능하게 하였다.
1. NTRODUCTION
지혈과 다른 장기의 누출(예; 뇌척수액, 담즙, 림프액, 위장관 분비, 뇨, 공기)을 보수하는 것은 수술 시 조직 관리와 밀접한 관계가 있다. 오늘날, 다음과 같은 기법과 기술로 누출 폐쇄(leak closure)와 지혈이 가능해졌다: [결찰(ligature), 봉합 같은 기계적인 조직 관리; 고주파(high-frequency), 압전기(piezoelectric), 광열기기와 같은 에너지 도구; 국소지혈제, 밀폐제 같은 생물학적 도구]. 이 연구의 목적은 표준화된 밀폐 시스템의 실험실적 모델에서 그 부착강도를 시험해 보는 데 있다.
2. MATERIALS AND METHODS
2.1. 생체 시뮬레이터
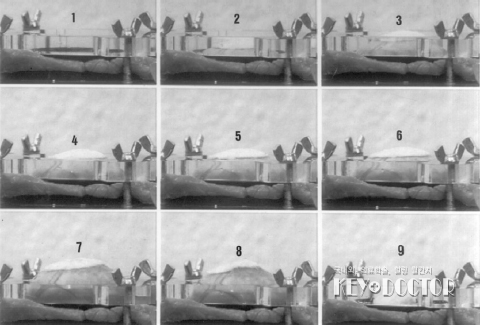
선택적 누출 폐쇄에 사용하는 생체재료의 부착강도를 평가하기 위해 플렉시글라스(PlexiglassⓇ) 재질의 정육면체 모양 챔버(길이 20cm, 부피 81)를 한 면은 주입구로 공기 공급이 가능하도록 하고 다른 한 면은 압력 측정이 가능하도록 만들었다. 생체막 혹은 합성막 위에 떼어낼 수 있는 덮개판(직경 6cm)과 플랜지(flange)를 밀폐되도록 원형틀을 돌려 고정하였다. 플랜지 위와 원형 틀 위에 고무 링을 끼워 확실히 밀폐하였다<그림 1>.

2.2. 막 재료
탄성과 같은 생체역학적인 특성과 조직학적인 디자인이 사람과 닮은 돼지늑막을 막의 재료로 사용하였다. 늑막재료는 -8℃에서 48시간동안 얼려 놓았고 실온에서 완전히 녹인 후 실험하였다. 준비된 막을 완전 밀폐상태로 원형틀 안에 넣은 후 금속 펀처를 이용해 막의 중앙에 직경 1cm의 표준화된 결함을 만들었다.
2.3. 접착제와 패치 재료
전통적인 수술과 최소침습수술(minimally invasive surgery, MIS) 모두에 사용되는 재료를 선택하였다.
액상 밀폐: 피브리노겐과 트롬빈을 적용하기 위해 피브린 접착제 BeriplastⓇHS(독일)를 배관(스프레이 밀폐)과 연결된 분출구로 주입하였다. 생분해성 합성 접착제 ADVASEALⓇ(미국)은 폴리에틸렌 글라이콜/폴리락티드/아크릴이스터의 광중합체이다.
플리스 밀폐: 이는 생체학적인 콜라겐이 준비된 상태로서 액상 밀폐를 증대시킬 수 있는 것이다. 이들은 플리스 폼(TachoTopⓇ, 오스트리아; Tissu-FleeceⓇE, 독일; SulmycinⓇImplant, 독일)이나 포일(TissuFoilⓇE, 독일)로서 대부분 말에서 추출한 재료들이 포함돼있다. 이들은 원하는 크기로 자를 수 있고 다양한 양의 피브린 접착성분(0.5-3.0mL)을 손으로 코팅할 수 있다(prepare-to-use). 콜라겐으로 코팅된 피브리노겐 기반의 즉시 사용 가능한(fibrinogen-based ready-to-use) 플리스인 TachoCombⓇH(오스트리아)는 조직 밀폐를 극대화하도록 발달시킨 제품이다. 이 제품은 피브리노겐/트롬빈의 성분이 섞이거나 감소될 염려가 없으며 사용 전에 미리 녹이거나 동결건조의 형태로 사용한다. 폴리글락틴 910(VicrylⓇ-Net, Ethicon GmbH), 폴리다이옥산(PDSⓇ, Ethicon GmbH) 같은 플리스 유사 합성 제품들이 있고 두 성분이 섞인 EthisorbⓇEthicon GmbH나 폴리글라이콜(PGA) 제품들이 있다. PGA net(BondekⓇ, 독일)는 통상적인 사용이 어려워 5x0 weaved 폴리글라이콜(BondekⓇ)에 작은 직조를 만들어(구멍크기: 0.1-0.3mm) 실험에 사용하였다. 비생분해성, 합성 재료들은 다양한 질감을 갖고 있으며 밀폐와 유사한 적용이 가능한 폴리테트라플루오로에틸렌(PTFE) 등이 포함된다.
2.4. 실험과정
생체 시뮬레이터는 디지털압력측정기(Membranovac, LH SOGEV, type MAC 2000)와 전자압력발생기(M4, Omron)에 연결하였다. 실험은 실온과 적당한 습도 등 보통의 조건에서 진행되었다.
Prepare-to-use: 피브린 접착제(BeriplastⓇHS)를 플리스 재료에 코팅하기 위해 분사 방법을 사용하였다(TachoCombⓇH와 동등). 금속펀처를 이용해 각 플리스 재료로 직경 30mm의 패치를 만든 후 패치 위에 직경 10mm의 표준화된 결함을 만들었다. Ready-to-use: 피브린 함유 콜라겐 플리스(TachoCombⓇH, 직경 30mm)는 생리식염수로 적시고 그 위에 결함을 만들었다. Liquid fibrin gluing: 늑막의 위치를 옮긴 후 표본에 구멍을 내고 결함 주변 30mm에 피브린 접착제(BeriplastⓇHS)를 분사하였다. 합성접착제(ADVASEALⓇ)를 목표 주변 30mm에 바른 후 5분 동안 쉬었다.
챔버 안에 압력을 가해 막에 편향이 생기거나 응괴(clot)나 플리스 재료에 변형이 생기도록 하였다. 응괴나 플리스 재료가 분리되거나 파괴되면 챔버 안의 압력을 감소시키고 도달한 최고 압력(hPa)을 각각 부착제의 강도로 하였다.
2.5. 통계
각 실험에서 10개의 측정을 하였고 통계적 유의성은 Kruskal-Wallis H-test와 Mann-Whitney U-test로 검증하였으며(SPSS, Version 6.1) 오차확률(p)이 0.05 미만이면 유의한 것으로 하였다.
3. RESULTS
챔버와 생체 시뮬레이터 안에 압력이 가해지자 순수 액상 밀폐인 BeriplastⓇHS와 ADVASEALⓇ은 접착면 반대가 분리된 후 밀폐가 파괴되었다. 각 개의 실험에서 플리스 기반 밀폐는 부착 드레싱이 유지되며 밀폐 층에서 플리스 재료가 분리되었으나 패치의 비가역적인 변형은 없었다<그림 2><그림 3>.

다양한 밀폐 시스템의 부착강도는 표와 같다<표>.
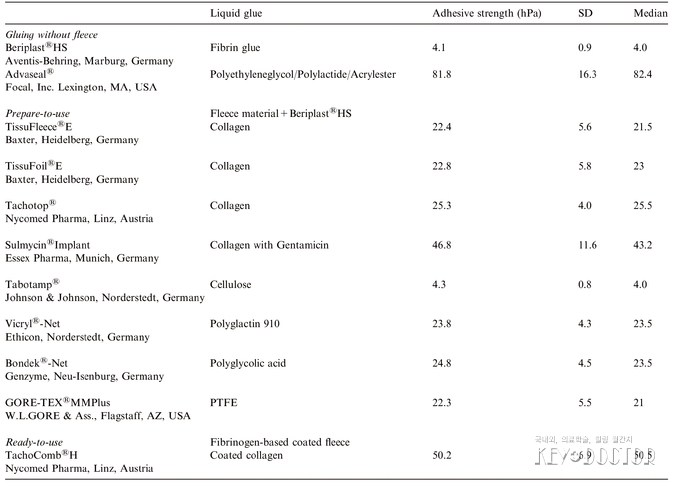
순수한 피브린 밀폐(분사 밀폐기법)는 셀룰로스 플리스 밀폐를 제외한 모든 플리스 밀폐에 비해 유의하게 낮은 강도를 나타냈다(p=0.004). 반면에 혼합된 합성부착제(ADVASEALⓇ)는 순수 피브린 밀폐와 모든 플리스 밀폐에 비해 유의하게 높은 강도를 나타냈다(각 p=0.004, p=0.007). 액상 피브린 밀폐와 비교 시 ‘ready-to-use’ 밀폐(TachoCombⓇH)는 망상의 변형된 부착층을 보이며 유의하게 높은 부착강도를 나타냈으나(p=0.004) ADVASEALⓇ에 비해서는 유의하게 낮은 강도를 나타내었다(p=0.02). TachoCombⓇH는 모든 ‘prepare-to-use’ 밀폐시스템에 비해 유의하게 높은 부착강도를 나타내었다(p=0.007).
4. DISCUSSION
이러한 밀폐제들은 자가제작 시험을 거쳐 1998년 FDA에서 승인을 받았다. 생화학적 스트레스 시험은 이런 평가에 유용하며 오늘날까지 다른 조건 하에서 이러한 연구들이 수행돼 왔다. Cronkite는 1944년 이미 부착된 피부 이식체에 대한 고정력 시험을 하였고 1990년 비슷한 모델에서 파열 력이 105.17-208.78g/cm2임을 알아내었다. 장기 문합에 대한 압력 시험이 피브린 밀폐와 유사하게 시행된 바 있었으나 사전에 시행된 봉합술로 인하여 높은 압력결과를 나타내어(435hPa, 294hPa) 이러한 유사제의 부착력이 확실한 것이라고는 인정하기 어렵다. 랫트의 폐 밀폐에 젤라틴-리소르시놀-포름알데히드 부착제를 사용한 생체실험에서 38hPa까지의 압력결과가 나온 바도 있다. 비장 병변의 밀폐에 대한 실험에서는 TachoCombⓇH의 실질에 대한 최고압력이 16.5mmHg(≡21.73hPa)로 나타나 콜라겐 플리스의 부착력에 대한 매개변수로 인용되고 있다. Agostini는 사람이 기침과 같은 강한 호기 시 압력이 118-225cm H2O에 달함을 발견하였다. 폐기종 같은 경우는 압력이 더 낮을 것으로 생각되며 이는 높은 부착강도를 보인 밀폐 시스템이 그런 병변의 밀폐에 효과적일 것이란 것을 알려준다. 이와 같은 전향적, 무작위 임상연구는 없었지만 임상적 관찰에 의하면 기흉이나 비장 파열 등에 대해 이러한 밀폐요법은 매우 효과적이다. 120mg의 겐타마이신을 주입한 TachoCombⓇH는 64.0hPa의 안정적인 부착력을 나타내어 부착제에 항생제를 주입하는 것이 부착 시스템에 손상을 가하지 않음을 입증하였다. Parker는 동물실험에서 리팜피신을 주입한 TachoCombⓇH의 지혈작용에 문제가 없음을 발견하였다. 그러므로 이러한 실험실적 평가모델을 생체모델에 적용할 수 있으며 임상적 관련성도 크다고 하겠다.
5. CONCLUSIONS
생체 시뮬레이터 안에서 액상 밀폐는 특별히 낮은 부착강도(피브린 접착제: 4.1hPa)와 높은 부착강도(광중합성: 82.9hPa)를 나타내었다. Prepare-to-use 기법의 플리스 재료들(플리스+피브린 접착제)은 각각 중간정도의 부착강도(6제품: 22.3-25.3hPa)를 나타내었고 Ready-to-use 기법의 TachoCombⓇH는 생체역학적으로 연관성 있는 높은 부착강도를 나타내었다(50.2hPa). 부착강도에 대한 지식은 임상에서 밀폐가 필요한 조직에 따라(역동적인 조직: 폐; 안정적인 조직: 간, 비장, 신장; 누출의 성격에 따름) 적용하면 되겠다. 액상 피브린 접착제는 낮은 부착강도로 인해 넓은 부위의 지혈보다는 결함의 밀폐에 더 적당하다. 생체 시뮬레이터는 생체막에 대한 밀폐 기술의 정확한 평가와 재현을 가능하게 하였으며 경제적이고 생태학적인 연관성이 있다.
REFERENCES













