염증성 장질환 치료제 킨텔레스, 피하주사 제형에 건강보험급여 적용
- 킨텔레스 정맥주사에 이어 피하주사 제형까지 보험급여 적용되며 치료 접근성 향상
- 킨텔레스 피하주사, 우수한 안전성 프로파일 확인된 정맥주사와 동등한 임상 관해 확인
한국다케다제약(대표 문희석)은 염증성 장질환 치료제 킨텔레스(성분명 베돌리주맙) 프리필드펜주(이하 킨텔레스 피하주사)에 12월 1일부터 건강보험급여가 적용된다고 밝혔다.
킨텔레스 피하주사(SC)는 환자가 병원을 방문하지 않고도 자가 투여할 수 있는 제형으로, 지난 2월 17일자로 킨텔레스주(이하 킨텔레스 정맥주사; IV)와 동일한 효능·효과로 국내 허가되었다. 킨텔레스는 정맥주사 1회 투여시간이 30분으로 짧다는 강점에 더해, 피하주사 제형까지 보험급여 치료 옵션으로 제공하며 환자들의 삶의 질을 한층 더 개선할 수 있게 되었다.1
한국다케다제약 김태훈 소화기사업부 총괄은 “킨텔레스가 생물학제제 중 유일하게 염증성 장질환만을 위해 개발된 약인 만큼, 염증성 장질환 환자의 맞춤형 치료 환경 조성을 위해 노력하고 있다”며 “우수한 치료효과와 안전성 프로파일을 가진 킨텔레스는 정맥주사와 피하주사 치료 옵션까지 제공하며 치료 편의성 향상에 기여하겠다”고 말했다.
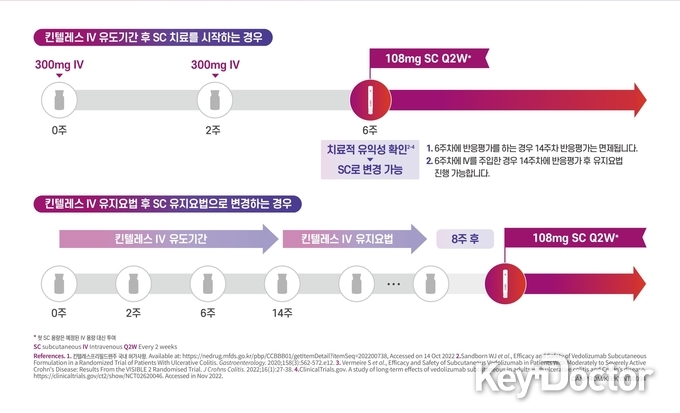
투여 방법은 ▲킨텔레스 300mg을 최소 2회 정맥주입 후 치료적 유익성을 보인 경우, 유지요법으로 킨텔레스 108mg을 매 2주마다 피하주사로 투여하거나 ▲킨텔레스 정맥주사 유지요법 투여 8주 후부터 킨텔레스 피하주사 108mg을 매 2주마다 유지요법으로 투여한다.1-3
보험급여 적용을 위해서는 첫 투여 후 14주 이내에 ▲환자가 ‘환자용 투약일지’를 작성하고 요양기관이 이를 관리하며 ▲장기처방 시 1회 처방기간은 퇴원 시 최대 2주분, 외래 시 최대 4주분을 원내 처방하고, 최초 투약일로부터 24주 이후에 안정된 질병활동도를 보이고 부작용이 없는 환자는 최대 8~12주분까지 인정한다.1
킨텔레스 피하주사는 VISIBLE 임상연구를 통해 정맥주사 제형과 동등한 임상적 관해 경향성을 보인 바 있다., 성인 궤양성 대장염 환자의 유지 치료에 대한 VISIBLE 1에서 피하주사는 유효성, 안전성 프로파일, 내약성 측면에서 정맥주사와 일치하게 개선된 환자 평가 결과를 보였다.4 성인 크론병 환자의 유지치료로 피하주사를 평가한 VISIBLE 2에서도 유의한 결과 개선을 확인하며 효과적인 치료 유지 효과를 보인 바 있다.5
킨텔레스는 중증도에서 중증의 활성 크론병 및 궤양성대장염의 치료에 쓰이는 생물학제제이다. 염증성 장질환 치료제 중 유일한 항인테그린제제로, 장에만 선택적으로 작용해 전신 면역을 억제하지 않는 우수한 안전성 프로파일을 보유하고 있다.2-
한편, 킨텔레스 정맥주사는 2020년 8월 1일부터 1차 치료제로 보험급여를 적용 받아, TNF-α 억제제 사용 경험과 상관없이 1차 치료제로 사용할 수 있다.3,
보건복지부 고시 제2022-262호 (2022년 12월 1일 시행)
킨텔레스프리필드펜주 국내허가사항. Available at https://nedrug.mfds.go.kr/pbp/CCBBB01/getItemDetail?itemSeq=202200738 (Accessed in Nov 2022)
킨텔레스주 국내허가사항. Available at https://nedrug.mfds.go.kr/pbp/CCBBB01/getItemDetail?itemSeq=201503975 (Accessed in Nov 2022)
Sandborn WJ, et al. Efficacy and safety of vedolizumab subcutaneous formulation in a randomized trial of patients with ulcerative colitis. Gastroenterology 2020;158:562-572.
Vermeire S, et al. Efficacy and safety of subcutaneous vedolizumab in patients with moderately to severely active Crohn’s disease: Results from the VISIBLE 2 randomised trial. J Crohns Colitis 2022 Jan 28;16(1):27-38.
Colombel JF, et al. The safety of vedolizumab for ulcerative colitis and Crohn's disease. Gut. 2017;66(5):839-851
보건복지부 고시 제2020-161호 (2020년 8월 1일 시행)












