
노을 마이랩, 미국 시장 진출 본격화∙∙∙美 FDA 첫 제품 등록 완료 ● 현재 논의 중인 미국 내 고객사 계약 위해 사전 등록 진행∙∙∙美 고객사 본격 확대 기대 ● 마이랩 솔루션별 FDA 승인 절차 순조롭게 진행 중∙∙∙“성공적인 미국 시장 진출 통해 세계적인 혈액 및 암 진단 전문 기업으로 도약할 것” 노을 주식회사(대표 임찬양, 이하 ‘노을’)는 미국 식품의약국(Food and Drug Administration, 이하‘FDA’)으로부터 시설 등록(Establishment Registration)과 자사의 의료기기 4개 품목(miLab™ Platform,miLab™Cartridge MAL, miLab™ Cartridge BCM, SafeFix™)에 대한 1등급 의료기기 제품 등록(Device Listing)을 완료했다고 밝혔다. 현재 노을은 본격적인 미국 시장 진출을 위해 마이랩 솔루션별 FDA 승인 절차를 각 단계별로 순조롭게 진행 중에 있다. 노을 임찬양 대표는 "이번 등록은 현재 논의 중인 미국 내 고객사 계약을 위해 사전에 진행했다. 노을의 모든 진단 제품의기반이 되는 마이랩 플랫폼에 대한 첫 FDA 등록을 완료함으로써 미국 진출에 첫 발을 내

SML바이오팜, 사우디아라비아 리야드에서 열린 RGMBS에서 mRNA 기반 차세대 치료 비전 발표… 글로벌 시장 확장 의지 다져 SML바이오팜은 2024년 11월 10일부터 12일까지 사우디아라비아 리야드에서 열린 ‘리야드 글로벌 의료 바이오테크 서밋(Riyadh Global Medical Biotechnology Summit, RGMBS) 2024’에 초청받아 그간의 연구 성과와 혁신적인 질병 치료 비전을 세계 각국의 투자자 및 기업들과 공유하며 협력확대를 모색했다고 밝혔다. 이번 서밋에서 SML바이오팜은 ‘mRNA 기반 치료제: 생체 내에서 작용하는 혁신적 치료 전략(mRNA-based therapeutics: Innovative strategies for treatment utilizing in vivo system)’을 주제로 발표해 업계 전문가와 행사 관계자들의 큰 관심을 받았다. 사우디아라비아는 2024년 ‘국가생명공학전략(National Biotechnology Strategy)’을 발표하며 2040년까지 글로벌 바이오 허브로 성장하겠다는 목표를 수립했다. 무함마드 빈 살만 왕세자가 주도한 이 전략은 2030년까지 중동 및 북아프리카(MENA)

애터미, SCIE급 국제학술지에 콜마BNH ‘HemoHIM’ 안전성 논문 추가 게재 애터미(Atomy)는 국내 대표 건강기능식품 ODM 기업 콜마비앤에이치(콜마BNH)가 개발·제조하고 자사가 판매하는 건강기능식품 ‘애터미 헤모힘(ATOMY HemoHIM)’의 주원료이자 식품의약품안전처로부터 개별인정형 원료로 승인받은 ‘헤모힘(HemoHIM)’의 추가 안전성을 확인한 논문이 독성학 분야의 SCIE급 국제학술지 ‘Toxicological Research’에 게재됐다고 29일 밝혔다. 이번 연구는 1회 투여 독성 테스트, 28일 반복 투여 독성 테스트, 13주 반복 투여 독성 테스트, 설치류 유전독성 테스트 등 다양한 테스트를 통해 HemoHIM의 잠재적 독성과 추가 안전성을 검증하는 데 중점을 뒀다. 그 결과 설치류 독성 테스트에서 HemoHIM을 하루 2000mg/kg 용량으로 투여했을 때 독성 효과가 관찰되지 않아 안전성을 입증했다. 이 연구는 OECD의 국제 표준 독성 시험 가이드라인을 준수했다는 점에서 특히 의미가 크다. 이러한 결과가 SCIE급 국제 저널에 게재됨으로써 HemoHIM의 안전성 검증에 대한 신뢰성이 더욱 높아지고, 지적 재산권 확보에도 기

멘탈테크 스타트업 닥터프레소, 우울증 조기 진단 관련 연구 국제 학술지 게재닥터프레소(대표 정환보)는 사용자가 작성한 일기 텍스트 데이터를 활용해 우울증을 감지하는 새로운 AI 기술을 개발했다고 밝혔다. 이번 연구는 전 세계적으로 증가하는 우울증의 조기 진단과 치료를 위한 혁신적인 접근 방식을 제시하고 있다. 해당 연구는 우수성을 인정받아 국제 학술지 ‘JMIR (Journal of Medical Internet Research)’ 9월호에 게재됐다. 우울증은 전 세계적으로 심각한 사회적 문제로, 직업 생산성 저하와 높은 장애 부담을 초래하고 있다. 하지만 기존의 우울증 선별 도구는 객관성과 정확성에 한계가 있어 이를 보완하기 위한 새로운 방법들이 필요했다. 이번 연구는 닥터프레소가 자체 개발한 일기 애플리케이션을 통해 확보한 사용자의 일기 데이터를 기반으로 우울증을 감지하는 AI 알고리즘을 개발하고, 그 유용성을 검증했다. 연구에 따르면 AI 기반 대형 언어 모델(LLM)인 GPT 3.5와 GPT 4.0이 사용자의 일기 텍스트를 분석해 우울증 위험을 효과적으로 감지할 수 있음을 확인했다. 특히 LLM 모델을 활용해 개발한 AI의 경우 텍스트 기반 우울증 감
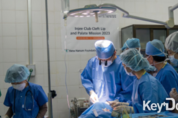
글로벌케어, 선천성 안면기형 수술팀 파견베트남·라오스 선천성 안면기형 아동 약 80명에게 무료 수술 국내 최초 국제보건의료 NGO인 글로벌케어(회장 박용준)는 오는 23일 베트남과 라오스 2개국 3개 지역(후에, 하노이, 사냐부리)에 7박 8일 일정으로 선천성 안면기형 수술팀을 각각 파견할 예정이라고 밝혔다. 배용찬 대장(부산대학교병원 성형외과)을 중심으로 경북대학교병원, 계명대학교동산의료원, 부산대학교병원, 분당서울대학교병원, 삼성서울병원, 순천향대학교병원, 세브란스병원, 영남대학교병원, 전남대학교병원, 아인성모이비인후과의원, 오늘성형외과의원, 원진성형외과의원, 이스트만치과, 참사랑 소아청소년과의원 총 14개 병원 전문의 및 간호사로 구성된 3개의 수술팀(총 32명)이 3월 23일부터 30일까지 베트남 후에와 하노이, 라오스 사냐부리로 각각 파견돼 약 80명의 선천성 안면기형 아동을 수술할 계획이다. 베트남에 파견될 두 팀은 배용찬 교수(부산대학교병원)를 팀장으로 하노이 박마이병원과 유대현 교수(세브란스병원)를 팀장으로 후에 대학병원, 라오스로 파견될 팀은 남승민 교수(순천향대학교 부천병원)를 팀장으로 사냐부리 주립병원에서 선천성 안면기형 아동의 수술을 진

미국이비인후과학회 참가 난청치료 연구성과 발표 - 소음성 난청 및 이독성 난청 치료 관련 연구 결과 소개 - □ 케이메디허브(대구경북첨단의료산업진흥재단, 이사장 양진영) 신약개발지원센터 이병현 연구원과 전임상센터 권태준 선임연구원이 2024년 미국이비인후과학회에서 난청치료 연구성과를 발표했다. ○ 미국이비인후과학회(ARO*)는 이비인후과 분야의 기초 및 임상연구 촉진을 위해 1973년 설립된 이비인후과 분야 세계 최대 규모 학회로 매년 초 학술대회(ARO Annual Midwinter Meeting)을 개최하고 있다. * ARO : Association for Research in Otolaryngology ○ 케이메디허브 이병현 연구원과 권태준 선임연구원은 각 ‘영구적 소음성 난청 마우스 모델에서의 덱사메타손 복강투여의 치료 효과’와 ‘Cyclophilin D 억제제를 이용한 감각신경성난청 보호 효과에 관한 세포학적 연구’ 주제를 발표해 소음성 난청과 이독성 난청의 치료 관련 연구성과를 알렸다. ○ 이번 발표는 현재까지 치료제의 개발이 이뤄지지 않은 난청 분야에서 난청의 원인에 따른 발생 기전과 치료제 개발의 가능성을 보여 주목받았다. ○ 이병현 연구원은
노바티스 CAR-T 치료제 ‘킴리아’, 미국혈액학회에서 최신 연구 데이터 3건 발표 ᄋ 2023년 미국혈액학회에서 킴리아 관련 의미 있는 최신 연구 데이터 발표 ᄋ 75세 이상 고령의 재발성 또는 불응성 미만성거대B세포림프종 환자, 실제 진료환경에서 75세 미만 환자와 유사한 객관적 반응률 및 완전 관해율 확인 ᄋ 재발성 또는 불응성 소포성림프종 환자 대상으로 진행한 ▲3년 추적 연구 결과, 고위험 하위그룹 포함 지속적이고 높은 반응률 확인, ▲7.3개월 추적 연구 결과 최적 반응률 97.5%, 전체 생존율 97.4% 확인 한국노바티스㈜(대표이사 사장 유병재)는 지난 9일부터 12일까지 진행된 미국혈액학회에서 자사의 CAR-T 치료제 킴리아(Kymriah: 티사젠렉류셀)의 실제 진료환경 내 연구와 장기 추적 연구 결과 등 총 3건*이 발표됐다고 13일 밝혔다.1,2 (*국내 허가 적응증 기준) 첫 번째 데이터는 국제 조혈모세포 이식 연구센터(CIBMTR)에 등록된 재발성 또는 불응성 미만성거대B세포림프종(이하 r/r DLBCL, Relapsed/Refractory Diffuse Large B Cell Lymphoma) 환자 1,375명을 대상으로 한 실제 임
노바티스 CAR-T 치료제 ‘킴리아’, 미국혈액학회에서 최신 연구 데이터 3건 발표 ᄋ 2023년 미국혈액학회에서 킴리아 관련 의미 있는 최신 연구 데이터 발표 ᄋ 75세 이상 고령의 재발성 또는 불응성 미만성거대B세포림프종 환자, 실제 진료환경에서 75세 미만 환자와 유사한 객관적 반응률 및 완전 관해율 확인 ᄋ 재발성 또는 불응성 소포성림프종 환자 대상으로 진행한 ▲3년 추적 연구 결과, 고위험 하위그룹 포함 지속적이고 높은 반응률 확인, ▲7.3개월 추적 연구 결과 최적 반응률 97.5%, 전체 생존율 97.4% 확인 한국노바티스㈜(대표이사 사장 유병재)는 지난 9일부터 12일까지 진행된 미국혈액학회에서 자사의 CAR-T 치료제 킴리아(Kymriah: 티사젠렉류셀)의 실제 진료환경 내 연구와 장기 추적 연구 결과 등 총 3건*이 발표됐다고 13일 밝혔다.1,2 (*국내 허가 적응증 기준) 첫 번째 데이터는 국제 조혈모세포 이식 연구센터(CIBMTR)에 등록된 재발성 또는 불응성 미만성거대B세포림프종(이하 r/r DLBCL, Relapsed/Refractory Diffuse Large B Cell Lymphoma) 환자 1,375명을 대상으로 한 실제 임
한국유씨비제약(대표이사 에드워드 리)이 4일 드라벳 증후군 치료제 핀테플라액(성분명 펜플루라민염산염; 이하 핀테플라)의 허가18를 기념해 기자간담회를 열고, 국내 드라벳 증후군 치료 환경 변화 필요성과 핀테플라의 임상적 의의를 소개했다. 이번 핀테플라 허가 기자간담회에는 연세대학교 세브란스 어린이병원 소아신경과 강훈철 교수와 분당서울대병원 소아청소년과 김헌민 교수가 연자로 참여해, 각각 국내 드라벳 증후군의 제한적인 치료 환경과 미충족 수요, 그리고 핀테플라 허가의 근거가 된 주요 임상 데이터를 중심으로 발표했다. 강훈철 교수는 <드라벳 증후군 질환 부담 및 미충족 수요>를 주제로, 드라벳 증후군의 질환 부담과 제한적 치료 옵션에 대해 설명했다. 강 교수는 “드라벳 증후군 환자는 다양한 발작 및 비발작 증상으로 인해 평생 심각한 신경발달, 운동, 인지, 행동 장애를 안게 되며[v],[vi] 돌연사(SUDEP) 등으로 조기 사망 위험이 매우 높고 사망 연령이 어린 것이 특징[vii],[viii],[ix]”이라며, 질환의 치명성에 대해 강조했다. 이에 강 교수는 “드라벳 증후군은 환자와 가족 모두에게 상당한 임상적, 경제적 부담을 초래하게 된다. 한

최근 건강검진이 활성화되면서 간 기능 이상을 조기에 발견하는 사례가 늘고 있다. 간 수치가 상승하면 일반적으로 바이러스 간염이나 지방간, 알코올성 간 질환을 먼저 의심한다. 하지만 이러한 원인으로 설명되지 않는 간 수치 이상이 일정 기간 지속된다면, ‘자가면역성 간염(Autoimmune Hepatitis, AIH)’을 의심해 볼 필요가 있다. 자가면역성 간염은 면역체계의 이상으로 자신의 간세포를 외부 물질로 인식하고 공격하면서 만성적인 간 염증을 일으키는 희귀난치성 질환이다. 특히 50대 이후 여성에서 발생률이 높은 것으로 알려져 있다. 건국대병원 소화기내과 최원혁 교수는 “바이러스 간염이나 지방간 등 흔한 원인이 배제됐는데도 간 효소 수치 상승이 지속된다면, 자가면역성 간염을 포함한 면역성 간 질환에 대한 평가가 필요하다”고 말했다. 무증상에서 전격성 간염까지… 다양한 임상 양상 자가면역성 간염은 만성 질환이지만 임상 양상은 매우 다양하다. 환자의 약 3분의 1은 별다른 증상 없이 지내다 건강검진에서 간 기능 수치 상승이 확인돼 정밀 검사 과정에서 진단된다. 특히 증상이 없다는 점이 진단을 지연시키는 요인이 되기도 한다. 실제로 자가면역성 간염 환자의 약

산업 발전을 위한 약가제도 개편 비상대책위원회(비대위, 공동위원장 노연홍·윤웅섭)는 한국노동조합총연맹(한국노총·위원장 김동명)과 산하 산별노조인 전국화학노동조합연맹(화학노련·위원장 황인석)이 비대위에 참여한다고 4일 밝혔다. 앞서 양측은 지난달 면담을 통해 정부의 약가인하 정책이 고용불안과 산업 기반 및 보건안보를 훼손할 수 있다는 데 공감대를 이룬 바 있다. 한국노총과 화학노련의 비대위 합류는 산업계와 노동계 양측 모두 약가인하 정책의 심각성에 대해 인식을 함께하고, 공동 대처하기로 뜻을 모았다는 데 의미가 있다는 평가다.

한국화이자제약(대표이사 사장 오동욱)은 지난 14일 자사의 경구용 코로나19 치료제 팍스로비드가 식품의약품안전처로부터 중증 신장애 환자를 대상으로 추가 승인을 받아 기존 적응증의 사용대상 환자군 사용범위를 확대했다고 밝혔다.1 이번 적응증 확대를 통해 혈액투석이 필요한 환자를 포함한 중증 신장애 환자(eGFR(추정사구체여과율) 30mL/min 미만)도 팍스로비드를 복용할 수 있게 됐다.1 중증 신장애 환자는 치료 첫날에는 니르마트렐비르 300mg과 리토나비르 100mg을 1회 복용하고, 2일차부터5일차까지는 니르마트렐비르 150mg과 리토나비르 100mg을 1일 1회복용하도록 권고된다.1 혈액투석을 시행하는 날에는 투석 후에 약물을 복용해야 한다.1 중등도 신장애 환자(eGFR 30 mL/min 이상 60mL/min 미만)는 기존 허가사항에 따라 니르마트렐비르150mg 1정과 리토나비르 100mg 1정을 하루 두 차례, 5일간 복용한다.1 코로나19가 엔데믹 국면에 접어들면서[i] 질환에 대한 경각심이 다소 줄어들었지만[ii], 코로나19 바이러스는 변이를 반복하며[iii] 여전히 환자가 지속적으로 발생하고 있다.[iv]특히 고령층 및 기저질환자 등 고위험군
